作成日:2024年5月17日
Prediction of tumor origin in cancers of unknown primary origin with cytology-based deep learning
目的:原発巣を細胞学に基づくディープラーニングによって予測する。
背景 :
CUPは病理学的に悪性転移と同定されるが、標準的な基礎診断アプローチではその起源を同定できない悪性疾患のグループである。CUPは人で診断される癌全体の3~5%を占めると考えられている。
免疫染色で同定される症例は30%未満であり困難な問題である。また腹水や胸水に遊離した腫瘍細胞が存在すると固有腫瘍のステージⅣの強力な証拠となる。
胸膜または腹膜の細針吸引による細胞診は通常、胸腹部転移の診断に重要な方法として用いられる。
研究内容:先行研究では、乳がんのリンパ節転移の検出、
前立腺がんのグリソングレーディングの予測、
胃がんの可能性の解釈などにAIモデルが利用されてきた。
しかしこれまでのモデルは組織学的な画像または全体画像に焦点をあたえたものであった。
なぜ細胞診は病理学的に難しいのか
細胞診は基本的に手術や針生検に耐えられない末期がん患者に適応される。その場合、胸水や腹水の検体はアクセス性に優れていて、がんの
発生部位を特定するのに有用である。しかしサンプリングの不適切さ、細胞の変性や異型性、検査者間のばらつきがあるため診断精度が最適でない。
原発不明癌の診断を難しくしているのは、そのとらえどころのなさである。
前処理
原発の臨床的または病理学的な裏付けを欠く、悪性腫瘍画像を除去する。空白または焦点の合わない画像を除外した。
トレーニングセット:
前処理をうけた19406枚の腫瘍画像と良性疾患の画像10477枚
テストセット:
・トレーニングセットを取得した病院と同じ四つの病院の10974人(12799画像)からなる3つの内部テストセット
・天津と煙台の病院からの外部テストセット
結果 : TORCHは癌診断でAUC0.953~0.991、腫瘍起源の特定で0.953~0.979を示した。強い汎化性能を示した
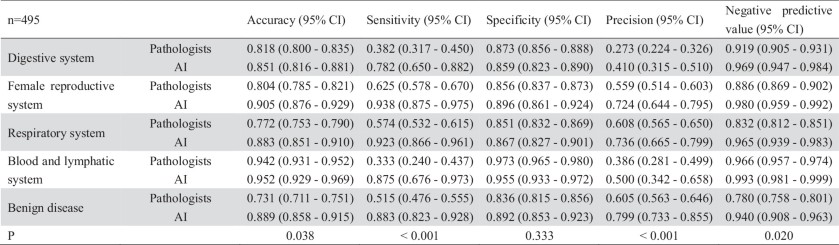
病理医との比較
若手病理医が42.6%(95%CI 38.2%-46.9%)と44.0%(95%CI 39.4-47.9%)、ベテラン病理医2名では69.7%(95%CI 66.3-73.5%)と57.0%(95%CI 52.9-61.2%)であったのに対し、
TORCHは78.8%(95%CI 75.4-82.0%)のトップ1精度を達成し、これは4人の病理医の精度を有意に上回った。
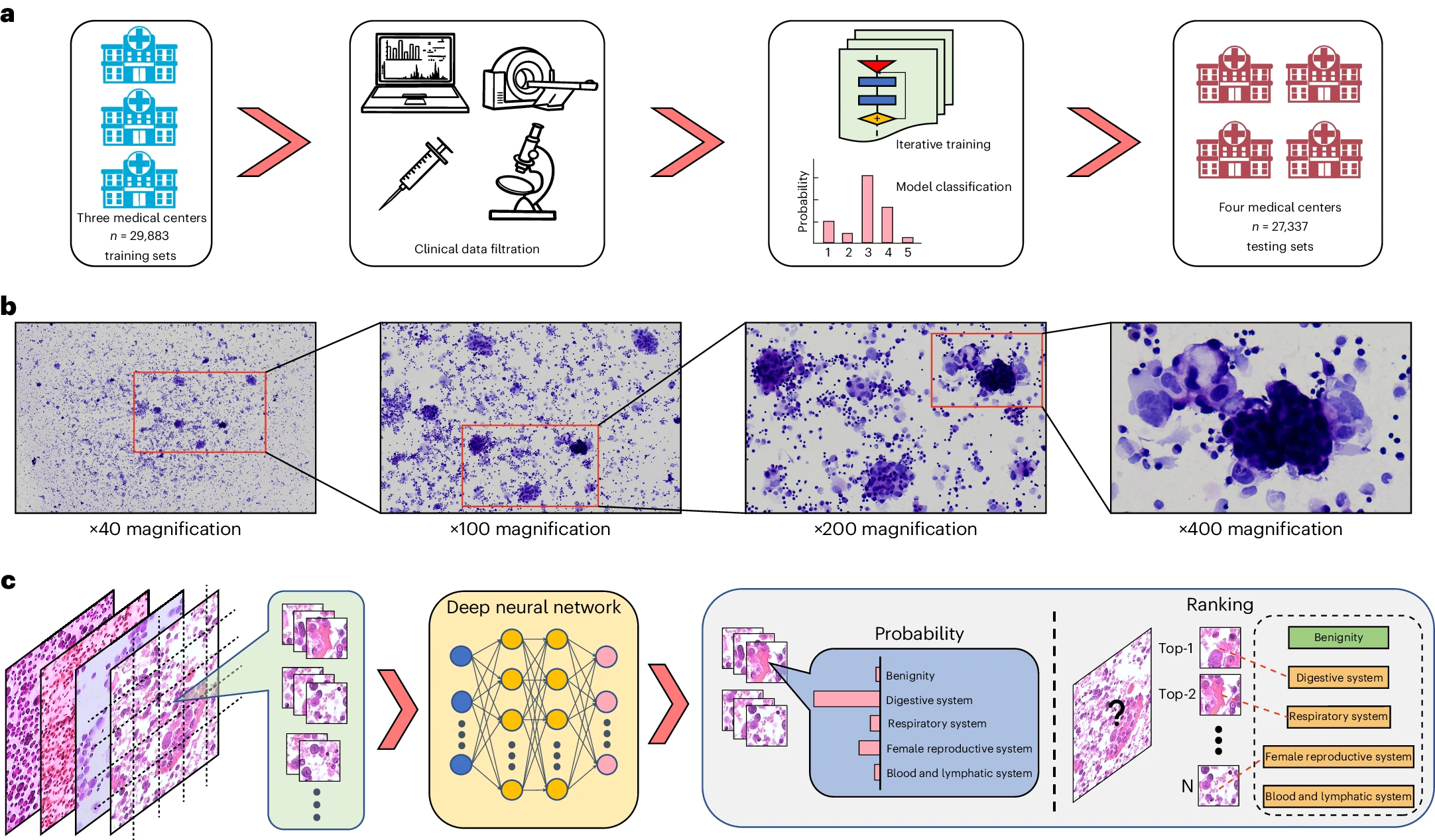
TORCHモデルフレームワーク
モデルの解釈性 : attention heatmapを利用して、モデルの予測結果を解釈した。
新規性:組織学的画像や全体画像ではなく、細胞学的画像データを解釈して腫瘍の起源を予測するAIモデルである点
感想:獣医療でもこういうAIが利用できるようになると、現場で病理検査に出すことなく、原発巣を予測することができ臨床的に非常に役立つと思った。
とくに悪性癌であれば進行が早いので迅速な診断ができるとかなり影響が大きいのではないかと思った。
参考リンク:
https://en.wikipedia.org/wiki/Ablation_(artificial_intelligence)
17 May, 2024
Prediction of tumor origin in cancers of unknown primary origin with cytology-based deep learning
Predict tumor origin using cytology-based deep learning
Background :
CUP is a group of malignant diseases that are pathologically identified as malignant metastases but whose origin cannot be identified by standard basic diagnostic approaches CUP is thought to account for 3~5% of all cancers diagnosed in humans.
This is a difficult problem because less than 30% of cases are identified by immunostaining. The presence of free tumor cells in ascites or pleural effusions is also strong evidence of stage IV endemic tumor.
Cytology by fine-needle aspiration of the pleura or peritoneum is usually used as an important tool in the diagnosis of thoracoabdominal metastases.
Research:There are previous studies that use the AI model. For example Detection of lymph node metastasis in breast cancer,
Predicting Gleason Grading of Prostate Cancer, and
Interpretation of the possibility of stomach cancer, etc.
However, previous models have focused on histological or whole images.
Why is cytology so pathologically difficult?
The cyst diagnosis is basically indicated for patients with terminal cancer who cannot tolerate surgery or needle biopsy. In such cases, pleural fluid and ascites fluid samples are highly accessible and
They are useful for localizing the site of origin of the cancer. However, diagnostic accuracy is suboptimal due to inadequate sampling, cellular degeneration and atypia, and inter-examiner variability.
What makes the diagnosis of cancer of unknown primary difficult is its elusive nature.
Preprocessing
Eliminated malignant tumor images that lack clinical or pathologic support for the primary tumor. Blank or out-of-focus images are excluded.
Training set:
19406 preprocessed tumor images and 10477 images of benign disease
Test sets:
・hree internal test sets consisting of 10974 individuals (12799 images) from the same four hospitals from which the training set was obtained.
・External test sets from hospitals in Tianjin and Yantai
Results : TORCH showed AUC 0.953~0.991 for cancer diagnosis and 0.953~0.979 for tumor origin identification. It showed strong generalization performance
Comparison with pathologists
TORCH achieved 78.8% (78.8%) accuracy, compared to 42.6% (95% CI 38.2%-46.9%) and 44.0% (95% CI 39.4-47.9%)
for the young pathologists and 69.7% (95% CI 66.3-73.5%) and 57.0% (95% CI 52.9-61.2%) for the two veteran pathologists
( 95% CI 75.4-82.0%) top 1 accuracy, which was significantly higher than the accuracy of the four pathologists.

TORCH Model Framework

Interpretability of the model
The attention heatmap was used to interpret the model's predictions.
Novelty
AI model predicts tumor origin by interpreting cytological image data rather than histological or whole images
Impression:
If this kind of AI can be used in veterinary medicine, it will be very useful clinically in predicting the primary tumor without sending the patient to pathological tests.
Especially in the case of malignant cancers, the rapid progression of the disease may have a significant impact if a quick diagnosis can be made.
Reffering Site:
https://en.wikipedia.org/wiki/Ablation_(artificial_intelligence)


